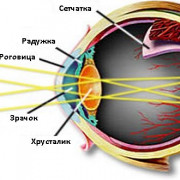
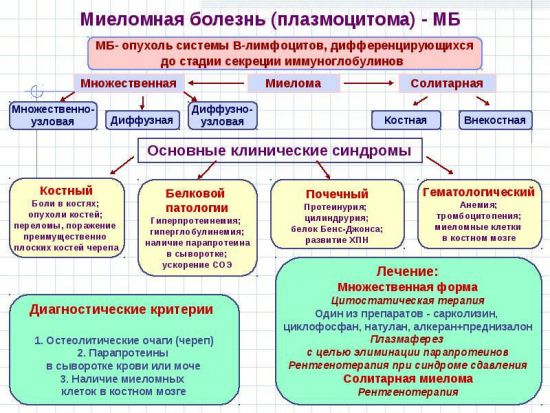
Миеломная болезнь
Содержание:
Что представляет собой миелома
Миеломная болезнь — злокачественное новообразование костного мозга, состоящее из атипичных плазматических клеток. Миелома считается опухолевой болезнью лимфатической системы низкой степени злокачественности. В настоящее время болезнь чаще классифицируется как плазмоцитома или множественная миелома.
В норме плазмоциты формируют иммуноглобулины, противостоящие попаданию и распространению инфекций в организм. При сбое этого процесса в костном мозге образуется миеломная клетка. При неблагоприятном течении мутирующая клетка активно размножается, образуя плазмобласты и плазмоциты, синтезирующие парапротеины — аномальные белки иммуноглобулина. Эти клетки уже не способны осуществлять иммунную защиту организма, но продолжают формироваться в тканях костного мозга.
Кроме этого миеломные клетки способствуют выделению цитокинов, выполняющих следующие функции:
- Провоцируют рост парапротеинов. Чем больше злокачественных клеток, тем быстрее развивается миелома, поражая другие органы.
- Убивают иммунитет. Организм не борется с атипичными клетками, вследствие этого он подвержен частому инфицированию бактериями.
- Миеломные клетки активируют размножение остеокластов — гигантских многоядерных клеток, разрушающих костную ткань, хрящи и образующих пустоты.
- Стимулируют образование фибробластов — клеток соединительной ткани, выделяющих фиброген и эластин, которые увеличивают вязкость крови.
- Благоприятствуют размножению печеночных клеток (гепатоцитов), нарушая выработку протромбина и фибриногена, приводя к плохой свертываемости крови.
- Развивают болезнь почек, нарушая метаболизм белков.
Миелома обладает низкой способностью размножения атипичных клеток, чаще поражающих костный мозг и кости, реже — лимфоузлы, лимфоидные ткани, почки, селезенку.
Как правило, миеломную болезнь характеризует медленное развитие. С момента образования атипичной клетки до появления явных признаков миеломы может пройти более 2-3-ех десятков лет. Если при ярко выраженной миеломной болезни не назначено грамотное лечение, она приобретает скоротечное течение, в течение 2-ух лет приводящее к смерти больного.
Формы плазмоцитомы
Формы злокачественного заболевания плазматических клеток могут быть представлены:
а) Солитарной формой, ограниченной отдельно развивающимися опухолями, преимущественно локализованными в плоских костях (миелома костей), вызывающей их разрушение. Внекостные и костные солитарные миеломы представляют очень небольшую группу опухолей, пребывающих в начальной фазе генерализованной плазмоцитомы, которых всего-то от 1 до 4%. Внекостномозговые солитарные опухоли можно встретить в носоглотке, желудочно-кишечном тракте и (очень редко) в веществе и оболочках головного мозга.
б) Генерализованным процессом, имеющим несколько разновидностей:
- Диффузная миелома характеризуется поражением костного мозга в результате начавшейся клоновой пролиферации (размножение): плазмоцитарной или плазмобластной;
- Диффузно-очаговая форма (диффузно-узловая), возникающая, когда поразившие костный мозг клетки пролиферируют в другие органы. В первую очередь страдают кости и почки, развивается миеломная нефропатия за счет циркулирующих PIg, которые, попадая в почечные канальцы, повреждают их и таким образом закрывают просвет;
-
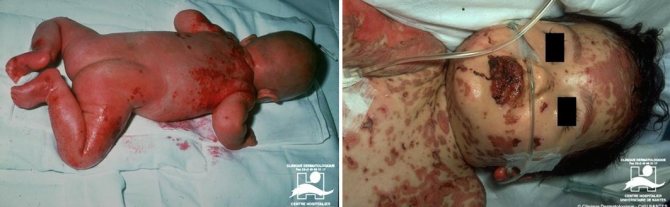
Множественная миелома, название которой уже указывает на генерализованное поражение всего организма, формируется в процессе расселения миеломных клеток с образованием опухолевых пролифератов в коже (миелома кожи) и внутренних органах;
Ввиду низкой встречаемости солитарной опухоли, нет особого смысла останавливаться на ней, поэтому дальнейшее описание заболевания будет подразумевать типы, клинические проявления и лечение множественной миеломы.
Иммунохимическая классификация подразумевает деление заболевания на формы в зависимости от принадлежности белков к определенному классу иммуноглобулинов и тогда, если белки относятся к IgE, то миелома называется Е-миеломой, к IgA – А-миеломой, к IgМ – М-миеломой и так далее. Клиническая симптоматика морфологические особенности клеток и ответ на лечение существенных различий в разных иммунохимических вариантах плазмоцитом не имеют. Правда, отдельные признаки той или иной разновидности в некоторых случаях отмечаются. Так, при D-миеломе хуже прогноз, чем при других формах болезни, к тому же, она больше свойственна для молодого возраста, чем, например, протеинурия BJ.
Дифференциальная диагностика миеломатоза
Симптоматика миеломатоза нередко напоминает проявление более распространённых заболеваний онкологического и доброкачественного генеза. Наибольшую сложность представляет дифференцирование признаков плазмоцитомы и доброкачественной моноклональной гаммапатии.
Доброкачественные гаммапатии также характеризуются образованием клонов иммуноглобулинпродуцирующих клеток, однако рост их количества не происходит или происходит очень медленно. Концентрация моноклональных иммуноглобулинов в сыворотке крови не превышает 3 г/дл, а доля плазмоцитов в костномозговой ткани составляет до 5 %. Поражения костей и гиперкальциемия не фиксируются.

Гаммапатия является наиболее частой причиной парапротеинемии (повышенного количества патологического белка в крови). По статистике, она наблюдается у 1-1,5 % людей старше 50 лет и у 3-10 % людей старше 70 лет. Это состояние не требует срочного лечения, но обязательно наблюдается врачами, т. к. в 16 % случаев оно способно развиться в миеломную болезнь, а в 17 % и 33 % (в течение 10 и 20 лет соответственно) – в другие виды гемобластозов. В половине случаев повышенное количество патологического белка наблюдается в течение всей жизни пациента, но не становится причиной его смерти.
Дифференциальная диагностика с другими причинами остеолитических повреждений (низкая секреция эстрогенов, болезнь Реклингаузена, старческий остеопороз, метастазы карциномы предстательной и щитовидной желёз) производится по анализу концентрации парапротеинов и миелограмме.
Схожесть с симптомами миеломы имеют и признаки болезни Вальденстрёма. Наблюдаются характерное повышение моноклональных иммуноглобулинов (IgM), избыточная выработка парапротеинов и повышенное количество лимфоплазмоцитарных клеток. Отличие заключается лишь в отсутствии литических поражений костей, что определяется на томографии.

Дифференциальная диагностика миеломатоза и других синдромов, связанных с парапротеинемией, проводится также при почечной недостаточности невыясненной этиологии.
Ранняя диагностика миелом возможна только при регулярном проведении общих клинических анализов и почечных проб (биохимии крови). Если пациент бережно относится к своему здоровью и ежегодно отслеживает динамику результатов, то у него есть все шансы обратиться к врачу задолго до появления клинических признаков миеломатоза и с помощью интенсивной терапии достигнуть длительной ремиссии заболевания.
https://youtube.com/watch?v=C3_xehhPMZM
Причины заболевания. Факторы риска
Причины развития миеломы достоверно неизвестны. Можно выделить лишь общие факторы, способствующие проявлению онкологических заболеваний в целом. Довольно часто миелома обнаруживается у людей пожилого возраста (старше 65 лет), людей, подвергающихся воздействию какого-либо ионизирующего излучения, имеющих длительный контакт с продуктами нефтепереработки, асбестом и другими токсическими веществами. Некоторую роль в появлении миеломы играют расовая принадлежность, вирусные инфекции, стресс и генетическая предрасположенность.
По статистике среди темнокожего населения миелома встречается почти вдвое чаще, чем среди белокожих наций, однако причину такого распределения до сих пор не смогли выявить.
Общая характеристика и особенности патологии
Плазмоцитома – гиперпластически-опухолевая патология, которая близка к лейкозам и располагается в костном мозге, поражая плазмоциты. Миелома может поражать кости позвоночника, ребер, таза, черепа, грудной клетки. В некоторых случаях ее обнаруживают в трубчатых костях. Новообразование имеет вид узелка, размер которого варьируется от 10 до 12 см в диаметре, мягкого по структуре. Расположение их неупорядоченно, находится в разных костях. Поражает миеломная болезнь чаще всего людей, старше 50 лет. Причем заболевание чаще встречается у мужчин, чем у женщин.
Плазмоциты – производящие иммуноглобулины клетки. Они необходимы для поддержания уровня иммунитета человека. Вследствие поражения их раком они перерождаются в плазмомиеломные клетки и начинают бесконтрольно делиться, производя при этом неправильные иммуноглобулины: lgG, А, М, D, Е. Данные белковые клетки не защищают организм от внешнего воздействия, так как неправильно работают. Также вследствие их большого количества, они разносятся по телу человека и накапливаются в различных органах, нарушая тем самым их деятельность. В некоторых случаях происходит синтезирование не целых иммуноглобулинов, а только часть цепи. Впоследствии их обнаруживают в анализе мочи, что дает возможность поставить диагноз.
Поражение плазмоцитомой приводит к тому что:
- увеличивается синтезирование пораженных плазмоцитов, тем самым снижая количество лейкоцитов, эритроцитов, тромбоцитов;
- нарушаются функции белкового и минерального метаболизмов, кроветворения;
- пониженный иммунитет и подверженность организма различным заболеваниям;
- увеличивается вязкость крови;
- происходят патологические изменения в кости – растущая опухоль истончает и разрушает костную ткань, прорастая через кортикальный слой поражает мягкие ткани.
Заболевание относится к системным, так как плазмоцитома проходит по всему организму и поражает все органы. Данные инфильтраты не всегда обнаруживаются при жизни пациента. Чаще всего их обнаружение происходит при вскрытии.
Причины
До конца причины возникновения данного заболевания ученым пока неизвестны, однако, есть сведения, что оно имеет генетическую предрасположенность. Кроме того, считается, что риск развития миеломного заболевания увеличивается под влиянием химических и физических канцерогенов, а также под воздействием радиоактивного облучения.
В группе риска:
- Мужчины. С возрастом концентрация мужских половых гормонов снижается, что может дать толчок к развитию заболевания. У женщин этот недуг диагностируется реже.
- Возраст. Среди всех больных миеломной болезнью только 1% приходится на людей младше 40 лет, возможно это связано с тем, что иммунитет у пожилых людей ниже, а, следовательно, уничтожение раковых клеток происходит хуже. Чаще заболевание диагностируется после 50 лет.
- Наследственность. В 15% случаях заболевания, родственники больного также страдают этой патологией. Это обусловлено мутационными процессами в гене, который отвечает за созревания определенных лимфоцитов.
- Лишний вес. Ожирение отрицательно сказывается на обменных процессах, что естественно понижает защитные функции организма и создает благоприятные условия для роста и развития злокачественных клеток.
- Облучение радиацией и влияние других отравляющих веществ. В этом случае риск мутации плазмоцита повышается, а это провоцирует образование миеломной клетки, которая становится началом опухолевого процесса.
Гиперкальциемия
Симптомы гиперкальциемии неспецифичны и зависят как от абсолютных значений, так и от сроков прироста кальция. Умеренная гиперкальциемия (кальций сыворотки 3–3.5 mmol/л), которая развивалась месяцами, может переноситься незаметно с минимальными жалобами , в то время как гиперкальциемия, возникшая за недельный период, приводит к ярким симптомам. Тяжелая гиперкальциемия ( кальций более 3.5 mmol/л) почти всегда приводит к клиническим проявлениям. Больные жалуются на отсутствие аппетита и запоры. При этом общее недомогание и мышечная слабость может прогрессировать до летаргии, спутанности и комы. Кардиоваскулярные проявления включают укорочение QT интервала и аритмии. Почечная дисфункция представляется другим важным проявлением гиперкальциемии. Пациенты часто отмечают полиурию как следствие пониженной концентрационной способности почек в условиях гиперкальциемии. Появление камней в почках наблюдается только при длительной гиперкальциемии. Острая почечная недостаточность в результате прямой вазоконстрикции и натриурез-вызыванное сокращение объема крови относится к наиболее тяжелым проявлениям поражения почек при гиперкальциемии. Причиной гиперкальциемии является повышенная активность остеокластов при пониженной активности остеобластов и лизис костной ткани при миеломной болезни. Активация остеокластов, разрушающих структуру костей, вызывается цитокинами, секретируемыми миеломными клетками, в частности , интерлейкином-1. Не случайно степень гиперкальциемии зависит от общей массы накопившихся миеломных клеток, так что наиболее тяжелая гиперкальциемия обнаруживается у больных с широко распространенной болезнью.
Признаки гиперкальциемии зависят от уровня кальция и быстроты его повышения, что создает необходимость в ускоренном обследовании. Большинство причин гиперкальциемии на практике обусловлено повышенным уровнем паратгормона и его производных (гуморальная форма), а в 20 % — с инфильтрацией костного мозга клетками опухолей (инфильтративная форма). Множественная миелома с легкими цепями в крови является самой частой причиной среди заболеваний крови. Число больных с гиперкальциемий из-за наличия опухоли в 2-3 раза выше, чем из-за первичного гиперпаратиреоза.
Для миеломной болезни с гиперкальциемией характерен низкий уровень паратгормона, фосфор находится в норме. При гуморальной форме гиперкальциемии обнаруживается повышенный уровень паратгормона, низкий уровень фосфора.
Что такое лечение множественной миеломы?
Существует не известное лечение, которое лечит множественную миелому. Тем не менее, существуют методы, позволяющие уменьшить возникновение и тяжесть симптомов и продлить жизнь. Терапия определяется на основании состояния пациента и группы по борьбе с раком, сделанной с использованием пациента. Команда, вероятно, будет включать как медицинского специалиста в лечении миеломы, так и врача-онколога, а также лучевого онколога и других консультантов. Онкологические медицинские сестры и другие сотрудники, вероятно, будут важными членами группы лечения.
Варианты лечения (лечения) часто включают комбинации лекарств, некоторые из которых назначаются в виде таблеток и других путем внутривенной инъекции. К ним относятся препараты, которые влияют или модулируют иммунную систему, стероиды и некоторые пероральные или инъекционные химиотерапевтические препараты. Они обычно используются в комбинациях. Может быть роль для высокодозной химиотерапии с последующим введением стволовых клеток костного мозга, называемых трансплантацией стволовых клеток или аутотрансплантацией. При определении того, следует ли делать такую трансплантацию, вступают в силу многочисленные факторы. Дополнительная информация может быть получена из Руководства по национальной комплексной онкологической сети (NCCN.org), которые обновляются не реже одного раза в год. Другие медицинские процедуры могут включать стероиды, бисфосфонатную терапию, переливание крови или тромбоцитов, аутотрансплантацию и / или плазмаферез и другую комбинированную терапию в зависимости от стадии заболевания отдельного пациента. Кроме того, исследователи используют метаанализ (систематическое объединение данных из отдельных исследований для разработки более значимого заключения) нескольких исследований, чтобы помочь определить лучшие протоколы лечения болезни.
Болезненные области повреждения кости можно лечить лучевой терапией. Во многих случаях сломанные кости могут быть хирургически восстановлены.
Существует много лекарств, используемых для лечения множественной миеломы. Следующие препараты часто используются в комбинации с дексаметазоном, иногда перорально или по IV, в зависимости от индивидуального состояния болезни пациента:
- Дексаметазон (Декадрон) — модуляция иммунных клеток
- Бортезомиб (Velcade) — ингибитор протеазы
- Леналидомид (Revlimid) — модуляция иммунных клеток
- Памидроновая кислота (Aredia) — ингибирует резорбцию кости
- Золедроновая кислота (Zometa) — ингибирует резорбцию кости
- Мелфалан (Alkeran) — алкилирующий агент, который токсичен для клеток миеломы
- Carfilzomib (Kyprolis) — ингибитор протеазы, который одобрен FDA обычно для пациентов, у которых не было предыдущего лечения
- Daratumumab (Darzalex) — моноклональное антитело, которое может повредить или убить несколько клеток миеломы (и других), которые имеют белок CD38 на их поверхности
- Elotuzumab (Empliciti) — соединение, которое активирует естественные клетки-убийцы тела для уничтожения нескольких клеток миеломы, обычно в сочетании с Revlimid и Decadron
Есть по меньшей мере семь или восемь других препаратов, которые иногда используются отдельно или в сочетании с переливанием, хотя эффекты переливания являются временными. Исследования продолжаются, и новые препараты и комбинации лекарств исследуются и используются для лечения с некоторой частотой. Большинство специалистов здравоохранения, специализирующихся на лечении рака, знают о новейших методах лечения множественной миеломы (например, Procrit, Revlimid, Kyprolis). Кроме того, ваш врач может устранить побочные эффекты (например, тошноту и рвоту с помощью химиотерапии), которые могут возникать при лечении. Одной из целей лечения является выживаемость без прогрессирования; то есть продолжительность времени и после лечения, что пациент живет без ухудшения симптомов. Кроме того, низкодозовая терапия препаратами изучается у пожилых пациентов с множественной миеломой.
Симптомы
Клиническая картина миеломы зависит от ее стадии. Около 10% случаев имеют скрытую симптоматику из-за отсутствия синтеза парапротеинов. Заболевание развивается медленно, с момента появления первых злокачественных клеток может пройти не один десяток лет, прежде чем появятся типичные признаки.
Сразу после возникновения симптомов течение болезни многократно ускоряется, и всего за 2 года она может привести к летальному исходу при отсутствии лечения. Наибольшему поражению подвергаются кости, почки и иммунитет, и наблюдается ряд характерных проявлений:
- боль в костях, обусловленная образованием полостей и раздражением болевых рецепторов, которыми весьма богата костная ткань. Особенно сильно кости болят при повреждении надкостницы;
- болевые ощущения в области сердца, суставов и мышцах связаны с тем, что в данных структурах накапливаются патологические белковые отложения. Из-за них нарушается работа органов, а чувствительные рецепторы реагируют болью;
- патологические переломы возникают как следствие разрежения костей и развития остеопороза. Кости приобретают несвойственную им хрупкость и могут сломаться даже от несильного толчка. Самыми уязвимыми являются бедренные кости, ребра и позвонки;
- иммунитет снижается вследствие сбоя в работе костного мозга, поскольку он секретирует мало лейкоцитов, и уменьшения числа нормальных иммуноглобулинов. В связи с отсутствием качественной защиты от инфекций человек чаще и дольше болеет ангиной, бронхитом или гайморитом. Сложность состоит в том, что эти вторичные болезни очень трудно поддаются лечению;
- избыток кальция, который поступает из разрушенных костей в кровь, вызывает задержку стула, боли в животе, тошноту, усиленное мочеотделение, нервные реакции, слабость и вялость;
- быстрая утомляемость и снижение концентрации внимания за счет уменьшения концентрации гемоглобина. При физических нагрузках учащается сердечный ритм, появляется одышка, головная боль, и бледнеет кожа.
Работа почек нарушается из-за кальциевых отложений в протоках и образования камней. Негативно влияет на почки нарушение белкового обмена: парапротеины, продуцируемые миеломными клетками, тоже откладываются в тканях почек. Орган сморщивается, возникает нефросклероз, отток мочи затрудняется, поскольку моча застаивается в почечных лоханках. Характерно, что при этом нет отеков, и не повышается артериальное давление.
Одним из симптомов миеломы является нарушение свертываемости крови и повышение ее вязкости, что способно привести к формированию тромбов. Из-за уменьшения концентрации тромбоцитов – тромбоцитопении – возможны внезапные кровотечения из носа или десен. При повреждении мелких кровеносных сосудов возникают подкожные кровоизлияния, и образуются синяки.
ВАЖНО: термины «миелома кожи» или «миелома почек» не вполне корректны, так как содержат характеристику, уточняющую местонахождение опухоли. Однако миелома всегда поражает костный мозг и кость, в которой он содержится
Подобное уточнение можно сравнить с выражением «масло масляное», описывающее избыточность определений.
Современная терапия миеломы
Терапия миеломной болезни включает следующие мероприятия:
- Лучевая и химиотерапия цитостатиками.
- Лечение миеломной болезни анаболическими стероидами и глюкокортикостероидами.
- Хирургическое и ортопедическое лечение.
- ЛФК.
- Профилактика метаболических нарушений.
Химиотерапия
Показаниями к проведению цитостатическому лечению являются выраженные симптомы заболеваний: патологические переломы, наличие болей, анемия, гиперкальциемия, синдром повышенной вязкости. При нарастании опухолевой массы, обострении сильных болей, росте количества патологических плазмоцитов медлить с началом терапии нельзя.
В день лечения необходимо будет пройти еще одно полное обследование, которое позволит врачу судить о стадии и форме опухолевого процесса. Для отдельных химиопрепаратов нужно исключить противопоказания. По результатам исследований врач сможет судить об эффективности лечения.
Первый этап химиотерапии включает применение препаратов циклофосфата, сарколизина, производных нитрозомочевины. Они эффективны, когда очаги опухолевого роста плазмоцитов имеют значение 2-10%.
Средства и схемы приема подбираются в индивидуальном порядке, поскольку нельзя предугадать, как будет реагировать рост опухоли на конкретный препарат
Некоторые препараты имеют серьезные противопоказания, их прием требует осторожности:
Ударные дозы химиотерапии противопоказаны при язвенной болезни, сахарном диабете, артериальной гипертензии.
Осторожно нужно принимать циклофосфан при циррозе печени и гепатите.
Сарколизин при наличии почечной недостаточности может привести к нежелательным последствиям.
Инфекции, сопровождающиеся острой почечной недостаточностью, могут усугубить ситуацию в сочетании с цитостатиками.
Цитостатическая химиотерапия основана на следующих принципах:
- подборе комплекса препаратов;
- использования оптимальной схемы, строго придерживаясь сроков проведения и дозировок;
- в случае прогрессирования процесса адекватный переход на другой препарат.
Лучевое облучение
При органических опухолях костей, миеломе узлов в мягких тканях костного мозга и позвоночнике, при угрозе патологических переломов назначается лучевая терапия. При терминальной стадии и невосприимчивости организма к химическим препаратам облучение является единственным средством помощи.
При инфекционных осложнениях актибактериальное лечение проводится по обычным правилам: подбор антибиотиков, посев биологических сред. Но нужно не забывать, что на фоне любой инфекции у пациентов с миеломой может возникнуть ОПН. Поэтому к антибиотикам добавляются кровезаменители, рекомендуется обильное потребление жидкости, проводится контроль суточного диуреза и артериального давления.
Соблюдение диеты
Специальной диеты, которая была бы разработана только для миеломной болезни, не существует. Врачи индивидуально рассчитывают рацион питания, учитывая распространенность процесса, результаты обследования.
Разрушение костей, возникновение остеопороза требует поступления в организм кальция, поэтому рекомендуются молочные продукты. Если развилась анемия, пища должна содержать железо и белок. Не лишним будет ввести в рацион печень и мясо. Почечная недостаточность является самой частой спутницей заболевания. Для больных миеломой из всех диет больше подойдет бессолевая диета (стол №7).
Народные средства
При наличии миеломной болезни народные средства в борьбе с ней могут служить только в качестве дополнения к основному лечению. Болезнь серьезная, лечить ее рецептами народной медицины не имеет смысла. Самодеятельность может привести к печальным последствиям. Любой прием трав, микстур должен быть согласован с лечащим врачом-онкологом.
Можно применять следующие рецепты:
В стакане кипятка заварить веронику лекарственную в количестве 1 ч. ложки. Настоять пару часов. Принимают за час до еды и спустя час после нее по 100 мл.
Если в стакане кипятка заварить 1 ч. ложку сухого донника лекарственного, можно получить целебный настой, который принимают перед едой по 50 мл.
Фитотерапевты считают, что миелома боится чернокорня лекарственного, лабазника вязолистного и окопника обыкновенного. Они продлевают жизнь, способствуют улучшению общего состояния, особенно полезны при вялотекущей форме, когда опухоль сосредоточена в костном мозге и не успела выйти за его пределы.
Прогнозировование и факторы риска при миеломе
«Международная система прогнозирования» (ISS. 2005) была разработана на основании данных естественного исхода заболевания значительной клинической группы больных и основана на исследовании бета-2 микроглобулина в динамике. Бета-2 микроглобулин повышен у 75% больных миеломной болезнью.
Выделено три уровня этого онкомаркера, которые связаны с длительной выживаемостью пациентов. Это позволяет определить несколько стадий заболевния.
- бета-2-микроглобулин менее 3,5 мг/л и альбумин более 35 г/л, средняя выживаемость 62 месяца,
- промежуточная между 1 и 3 стадиями, средняя выживаемость 44 месяца.
- бета 2-микроглобулин более 5.5 мг/л, средняя выживаемость 29 мес.
Однако, в настоящее время использование новых препаратов значительно изменило прогноз естественного течения заболевания. Тем не менее, международная система была протестирована для новейшей терапии и подтвердила свою надежность. Так, 5-летняя выживаемость больных в стадии I, II и III составила 66%, 45% и 18% соответственно.
В Международной системе не оказалось места для таких ценных прогностических показателей как число тромбоцитов, уровень лактатдегидрогеназы и свободных легких цепей в крови.
Число тромбоцитов в крови коррелирует с вытеснением костного мозга и имеет предсказательное значение выше, чем у альбумина. Содержание лактатдегидрогеназы (ЛДГ) коррелирует с общей массой миеломных клеток, недостаточным ответом на терапию и укорочением выживаемости. У больных с уровнем свободных легких цепей в крови свыше 4,75 г/л чаще выявляется почечная недостаточность, высокой процент миеломных клеток в пунктате костного мозга, высокие значения бета-2-микроглобулина и лактатдегдрогеназы, чаще обнаруживается болезнь отложения легких цепей и стадия III по Международной системе. Однако представленных доказательств оказалось недостаточно, чтобы включить эти три критерия в Международную систему. Но они были представлены в системе Дьюри-Саймона (1975), значение которой не оспаривается до сих пор.
Повышенный уровень сывороточного бета 2-микроглобулина, повышенный уровень лактатдегидрогеназы и низкий уровень сывороточного альбумина относятся к неблагоприятным признакам прогноза при миеломной болезни. Хотя уровень бета-2- микроглобулина увеличивается при почечной недостаточности, существует значительная корреляция между объемом опухолевой ткани и концентрацией этого биомаркера в крови. Исключение составляют лишь случаи, когда миеломная болезнь развивается уже на фоне имеющейся почечной недостаточности.
Перспективным методом оценки прогноза заболевания является генетическое исследование опухоль-ассоциированных генов. Цитогенетическое выявление транслокаций в отличие от трисомии относится к неблагоприятным прогностическим признакам. Метод флюоресцентной гибридизации in situ (FISH) позволил упростить выявление хромосомных аберраций в миеломных клетках, что предлагается исследователями клинико Мэйо (США) использовать для выбора индивидуальной лечебной тактики, исходя из прогноза для больного на основании учета выявленных аберраций. Генетические исследования хромосомных аномалий и мутаций при миеломе являются перспективными методами для лабораторной оценке прогноза и устойчивости к терапии при миеломе. Однако для их оценки требуются большие сроки и число пролеченных больных, чтобы определить способность новых средств терапии преодолеть цитогенетические показатели высокого риска при миеломной болезни.
Стадии
Макроскопическая картина множественной миеломы зависит от степени поражения отдельных костей. В первоначальной стадии ни костная ткань, ни кортикалис, ни спонгиоза не обнаруживают изменений формы и консистенции, только костный мозг частично замещается серо-беловатой тканью, которая состоит из миеломных клеток. Рентгеновская картина в этой стадии практически не обнаруживает никаких изменений. И в дальнейшей стадии при макроскопическом наблюдении не видно на наружных контурах кости никаких бросающихся в глаза изменений, но консистенция пораженных костей мягкая, пораженную кость можно резать ножом. Кортикальный слой кости со стороны костного мозга бывает истончен, трабекулы спонгиозы редуцированы и также истончены. Костный мозг в большей части заменен серо-белой миеломной тканью, которая местами образует большие или меньшие изолированные опухолевые узлы. Эти изменения яснее всего видны при вскрытии на распилах костей.
 Фото множественной миеломы костей черепа
Фото множественной миеломы костей черепа
В следующей, более поздней стадии, миеломная опухолевая ткань в виде очагов узурирует кость, приподнимает надкостницу, после чего ее разрушает; опухоль прорастает в соседнюю ткань. Часто не только на черепе, но и на других костях возникают остро ограниченные, как будто выбитые железом дефекты. Эти костные дефекты являются очень характерными для миеломатоза, но могут встречаться и при иных поражениях, как, например, при остеолитических костных метастазах рака.
В связи с множественной миеломой необходимо вспомнить так называемую солитарную миелому. Речь идет о солитарном костном поражении, которое при гистологическом исследовании дает картину миеломы. Это заболевание иногда продолжается очень длительное время, даже несколько лет, однако все же в большинстве случаев переходит в диффузный миеломатоз.
В некоторых случаях множественной миеломы развивается атипический амилоидоз (парамилоидоз). Амилоид может лежать прямо в опухолевой ткани или же в соединительной ткани и в мускулатуре около кости и суставов, главным образом плечевого и тазобедренного, в виде мощного симметрического опухания. Атипический амилоид может локализоваться и во внутренних органах, особенно в пищеварительном тракте, в миокарде и в легких. Обыкновенно опухолевая атипия клеток проявляется в полиморфии, в частности изменяются величины протоплазмы и ядер.