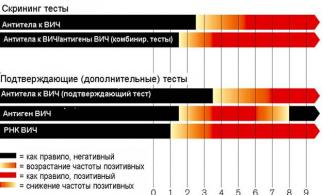
В россии создают тест на определение т-клеточного иммунитета к коронавирусу
Содержание:
Особенности барьерной иммунной на разных уровнях
Строение мукозальной иммунной системы в разных частях организма достаточно сильно отличается. Это обусловлено специфическими условиями функционирования различных органов.
Дыхательный тракт
Основой барьерного иммунитета ЛОР-органов и дыхательных путей является глоточное кольцо. Оно состоит из нескольких скоплений лимфатической ткани:
- Глоточная миндалина;
- Язычная;
- Трубные миндалины;
- Небные.
Часть из них (небные, язычная) имеют в своем составе ветвящиеся углубления – крипты. Они значительно увеличивают площадь поверхности миндалин, являются основным местом взаимодействия иммуноглобулинов и других факторов барьерного иммунитета с микробами. Еще одна важная особенность этих органов – наибольшая концентрация В-лимфоцитов среди всех лимфоузлов.
Эти клетки вырабатывают IgA и G, которые выделяются в пространство крипт и на слизистую оболочку миндалин.
Еще один важный компонент барьерного иммунитета дыхательной системы – эпителиальный слой, который содержит множество иммунных клеток (Т и В лимфоциты, макрофаги). Такое строение сохраняется вплоть до нижних отделов легких. В них в эпителии начинают преобладать М-клетки и клетки, продуцирующие слизь. М-клетки выполняют важную функцию – транспортируют внутрь организма часть антигенов в неизменном виде. Это позволяет формировать «системный» ответ, что играют большую роль в формировании устойчивости ко многим заболеваниям.
Ротовая полость и ЖКТ
Полость рта выстилает многослойный эпителий, который выделяет большое количество слизи. Это препятствует развитию патогенных микробов. Слизь также содержит иммуноглобулины и другие факторы мукозального иммунитета.
Важной частью барьерной системы рта являются слюнные железы. Слюна содержит достаточно большие концентрации лизоцима, иммуноглобулинов и других веществ, которые связывают и подавляют развитие патогенных микроорганизмов
Нарушение состава либо выработки слюны является одним из основных факторов, приводящих к развитию кариеса, который вызван условно патогенными микробами, поселяющимися на эмали зуба.
Большую часть кишечника выстилает однослойный ворсинчатый эпителий. В его состав входят вырабатывающие слизь клетки, лимфоциты, М-клетки. Также большую роль в защите кишечника играют лимфатические скопления, к которым относят
- Пейеровы бляшки;
- Фолликулы толстой кишки;
- Аппендикс;
- Диффузная лимфоидная ткань в стенках желудка и пищевода.
Немаловажную роль играют, и симбиотические бактерии, обитающие преимущественно в толстом кишечнике. Это важный фактор иммунной защиты, без них нормальное функционирование пищеварительной системы и мукозального иммунитета было бы невозможным.
Урогенитальная систем
В целом функционирование барьерного иммунитета мочеполовых органов схоже с другими частями этой системы. Но есть ряд особенностей:
- Нет крупных лимфатических скоплений;
- Количество клеток иммунной системы ниже чем в других отделах;
- В составе слизи преобладают IgG, количество IgA невелико;
- Большое количество лактобацилл на поверхности эпителия.
Особенно много лактобактерий находится на поверхности эпителия влагалища. Именно они формируют кислую среду и выделяют ряд антибиотических веществ, которые препятствуют развитию патогенной микрофлоре в этом органе.
Кожа
Основа защитной системы кожных покровов – многослойный эпителий клетки которого при отмирании формируют практически непроницаемый защитный слой. На его поверхности обитает множество микроорганизмов (более 100 разновидностей). Они создают среду неблагоприятную для развития болезнетворных бактерий.
Дополнительными факторами защиты служат выделения сальных и потовых желез. Они содержат лизоцим, иммуноглобулины и другие защитные вещества.
Нормальные показатели
Если у пациента повышен ИРИ, то это может быть признаком серьезных заболеваний. Однако невозможно поставить диагноз только лишь по данным иммунограммы. В данном случае необходимо пройти дополнительное обследование. При аутоиммунных патологиях больному показан длительный прием кортикостероидов и иммуносупрессоров, а также диспансерное наблюдение.
Что делать, если ИРИ снижен? Такой показатель является признаком ослабления защитных сил организма. Существуют ли препараты для повышения иммунорегуляторного индекса? Если снижение ИРИ спровоцировано инфекционной патологией или хроническими болезнями, то иммунитет самостоятельно приходит в норму после выздоровления или достижения ремиссии. В некоторых случаях пациентам назначают иммуномодуляторы:
- «Виферон»;
- «Полиоксидоний»;
- «Арбидол»;
- «Иммунал»;
- «Циклоферон».
Однако такие препараты можно принимать только по назначению и под контролем врача. Со временем организм привыкает к иммуномодуляторам, и эффективность таких лекарств уменьшается. Злоупотребление иммуностимулирующими препаратами может привести к истощению собственной иммунной системы.
Увеличение IgA происходит при хронических болезнях печени, аутоиммунных заболеваниях, миеломе, гломерулонефрите, алкогольной интоксикации. Снижению концентрации иммуноглобулина А способствуют физиологические изменения у ребенка до 6 месяцев, циррозное поражение печени, лучевая болезнь, терапия иммунодепрессантами, отравление организма химическими веществами.
Рост содержания IgG отмечается при аутоиммунных заболеваниях, миеломе, ВИЧ-инфекции, мононуклеозе инфекционной этиологии, инфекционных патологиях. Снижение иммуноглобулина G происходит в результате физиологических изменений у ребенка в возрасте до 6 месяцев, лучевой болезни, отравления химическими веществами, терапии иммунодепрессантами.
Антинуклеарные антитела повышаются при аутоиммунных патологиях, нефрите, хроническом гепатите, васкулите. Показатель АСЛО растет при острой форме гломерулонефрите, ревматизме, рожистом воспалении, скарлатине и инфицировании стрептококками. Антиспермальные антитела повышены при риске бесплодия. Показатель MAR-теста увеличен при вероятном бесплодии мужчины. Показатели АТ-ТГ и АТ-ТПО увеличиваются при аутоиммунном тиреоидите, болезни Грейвса, синдроме Дауна и Тернера.
Анализ на ЦИК (циркулирующие иммунные комплексы) назначают при: обследовании на наличие аутоиммунных патологий и дефицита комплемента, иммунопатогенетических поражениях почек, артритах различной этиологии, персистирующей инфекции. Циркулирующие иммунные комплексы повышены при остром инфицировании организма, персистирующей инфекции, аутоиммунных патологиях, аллергическом альвеолите, гломерулонефрите в острой форме, местной анафилаксии, сывороточной болезни, эндокардите, злокачественных опухолях, болезни Крона. Также циркулирующие иммунные комплексы исследуют в рамках общего иммунологического обследования.
Гуморальный
В отличие от клеточного, итогом гуморального иммунного ответа является выработка специфических антител – иммуноглобулинов. Это сложные белковые молекулы, которые при соединении со специфическими антителами связывают или уничтожают их.
Начало процесса общее с клеточным ответом – захват антигена антигенпрезентирующими клетками и его обработка. Но далее процесс кардинально отличается, в него входят следующие этапы:
- Передача обработанного антигена В-лимфоцитам;
- Распознавание конкретного участка-мишени в молекуле антигена;
- Активация лимфоцитов;
- Массивное размножение активированных лимфоцитов;
- Созревание новых поколений активированных лимфоцитов, передача информации об антигене в «клетки памяти»;
- Уничтожение попавших в организм антигенов.
Весь процесс занимает достаточно много времени (от нескольких дней, до недель и даже месяцев). Это связано с высокой сложностью проходящих в организме реакций. Иммунной системе требуется достаточно много времени для анализа антигена, создания соответствующего антитела и наращивания достаточного количества В-лимфоцитов.
В процессе гуморального ответа развиваются неспецифические реакции, такие как повышение температуры тела, другие симптомы заболевания. Они нужны для:
- Создания неблагоприятных условий для развития вирусов и бактерий;
- Ускорения обменных процессов в иммунных клетках, что сокращает период размножения В-лимфоцитов, увеличивает количество продуцируемых антител.
В норме процесс завершается полным уничтожением антигена и формированием иммунитета, то есть устойчивости к возбудителю, вызвавшему реакцию. Он может быть пожизненным, длительным (десятки лет) либо кратковременным (до 1 года).
В некоторых случаях защита организма от возбудителя не формируется, например, при патологиях иммунной системы либо при высокой способности возбудителя к мутациям.
Виды иммунного ответа
Исходя из механизмов, которые участвуют в его реализации, иммунный ответ может быть различным.
Неспецифический иммунный ответ – первичное состояние борьбы с инфекцией, которое возникает в случае попадания микроба в организм человека. Он практически одинаков для всех враждебных микроорганизмов и выражается в первичном разрушении микроба и формировании очага воспаления, что является универсальным защитным процессом, направленным на предотвращение размножения инфекции. Неспецифический иммунитет влияет на общее сопротивление организма. Если иммунитет человека ослаблен, он чаще болеет различными заболеваниями, такими, как ОРЗ, аллергия и пр.
Специфический иммунный ответ является вторичной защитной реакцией организма. Основным свойством данного иммунного ответа служит распознавание микроорганизма и выработка защитных факторов, направленных непосредственно на него.
Специфический иммунный ответ, в свою очередь, делится на два типа: клеточный и гуморальный.
Клеточный иммунный ответ выражается в формировании клона лимфоцитов, которым свойственно разрушать клетки-вредители, в мембранах которых содержатся чужеродные материалы (допустим, вирусные белки). Этот тип иммунитета участвует в уничтожении вирусной инфекции, а также туберкулеза, проказы, риносклеромы.
Гуморальный иммунный ответ опосредован В-лимфоцитами, которые после идентификации микроба активно синтезируют антитела по следующей схеме: на один тип антигена вырабатывается один тип антитела. При этом один микроб может переносить большое количество различных антигенов, в связи с чем организм вырабатывает целую серию антител.
Антитела (иммуноглобулины, Ig) – это белковые молекулы, пристраивающиеся к конкретной структуре микроорганизма, с последующим его разрушением или скорейшим выведением наружу. Различают несколько типов иммуноглобулинов, каждый из которых выполняет отведенную ему функцию.
Иммунитет: зачем он нужен?
Иммунная система отвечает за антигенный гомеостаз. В принятой в науке терминологии иммунитетом именуют невосприимчивость к определенному типу патологических микроскопических форм жизни и продуктов их жизнедеятельности, а также ядов, генерируемых животным. Иммунная система принимает участие в опознании и деструкции самых разных клеточных структур – бактерий и вирусов, паразитарных, простейших, грибковых, опухолевых. Иммунный ответ, возникающий при этом – это реакция на инвазию.
Эволюция – особенность, присущая любой форме жизни, но особенно ярко она прослеживается, если наблюдать за микроорганизмами. Свойства микроскопических форм жизни постоянно совершенствуются, и единственным эффективным ответом на это со стороны макроорганизмов оказалось формирование иммунитета разных видов. Впрочем, иммунитет не единственное, что защищает человека. Немалую роль играют факторы, не допускающие инвазию. К примеру, проникновение патологической микрофлоры в человеческий организм затруднено за счет эпителиальных ресничек, кожных покровов, слизистых, а также высокой кислотности желудочной среды.
Разновидности иммунитета
Медики различают два главных типа иммунитета: видовой (наследственный) и индивидуальный (приобретенный).
Видовой иммунитет присущ всем представителям животного мира. При этом видовой иммунитет человека гарантирует его безразличие относительно многих заболеваний фауны (к примеру, чума у собак), и наоборот, животным не причиняет вред целый перечень заболеваний человека. Видовой иммунитет передается от одного поколения к другому генетически по наследству.
Индивидуальный иммунитет развивается в течение жизни каждого человека и не переходит наследникам. Это, как правило, происходит в период заражения инфекцией или интоксикации организма, однако существуют болезни, которые угнетают иммунитет. К примеру, после перенесенной гонореи иммунитет человека ослаблен, поэтому спустя некоторое время может произойти повторное инфицирование. А, к примеру, ветряная оспа, наоборот, оставляет иммунитет стабильным, способным предотвратить повторное заражение в течение жизни.
Подробнее о Т-лимфоцитах
Это клетки, представляющие собой особый вид лимфоцитов, вырабатывающихся в тимусе. У людей так называется вилочковая железа, располагающаяся в грудной клетке чуть ниже щитовидки
В названии лимфоцитов использована первая буква этого важного органа. В костном мозге продуцируются предшественники Т-лимфоцитов
В тимусе происходит их окончательная дифференциация (формирование), в результате которой они приобретают клеточные рецепторы и маркеры.
Т-лимфоциты бывают нескольких типов:
- Т-хелперы. Название образовано от английского слова help, что означает «помощь». «Хелпер» на английском – это помощник. Такие клетки сами чужеродных агентов не уничтожают, но активируют выработку клеток-киллеров, моноцитов, цитокинов.
- Т-киллеры. Это «прирожденные» убийцы, цель которых – уничтожить клетки собственного организма, в которых поселился чужеродный агент. Этих «киллеров» существует множество вариаций. Каждая такая клетка «видит» только на какой-либо один вид патогенна. То есть Т-киллеры, реагирующие, например, на стрептококк, оставят без внимания сальмонеллу. Также они «не заметят» чужеродного «вредителя», проникшего в тело человека, но пока свободно циркулирующего в его жидких средах. Особенности действия Т-киллеров дают понять, чем клеточный иммунитет отличается от гуморального, работающего по другой схеме.
- γδ Т-лимфоциты. Их образуется очень мало, по сравнению с другими Т-клетками. Настроены они на распознавание липидных агентов.
- Т-супрессоры. Их роль – обеспечить иммунный ответ такой продолжительности и такой силы, которые требуются в каждом конкретном случае.
Что показывает иммунологическое тестирование?
Список показаний для проведения иммунограммы:
- Первичные иммунодефицитные состояния — это иммунодефициты, появившиеся вследствие генетического фактора или врожденные;
- Вторичные иммунодефициты — возникают из-за болезней органов иммунной системы — разновидности раковых заболеваний крови. В некоторых случаях причиной появления приобретенного иммунодефицитного состояния становится прием сильнодействующих лекарственных препаратов, назначенных строго по необходимости, или вследствие воздействия на организм радиоактивного излучения;
- Паразитарные инвазии — особенно при появлении у пациента гельминтов;
- Инфекционное поражение пищеварительной системы с симптомами снижения массы тела;
- Патологическая выработка аутоиммунных антител;
- Воспалительные болезни хронического характера — бронхит, синусит, гайморит;
- Вирус иммунодефицита человека;
- Аллергия;
- Онкология;
- Микозы — грибковые поражения;
- Пиодермия — поражение кожи гнойными кокками;
- Болезни вирусной этиологии;
- Длительный прием иммунодепрессивных препаратов — лекарственных средств, угнетающих работу иммунной системы;
- После трансплантации органов и тканей;
- После курса химиотерапии.
Забор крови на иммунограмму у детей Иммунограмма помогает подобрать правильное и эффективное лечение заболеваний различного характера, что особенно важно во время беременности, ведь в процессе вынашивания ребенка иммунитет женщины ослабевает, что способствует развитию множественных патологий. Показания для взятия венозной крови для иммунного тестирования во время беременности — это:
Показания для взятия венозной крови для иммунного тестирования во время беременности — это:
- иммунологическая несовместимость резус-отрицательной мамы и резус-положительного малыша, характеризующаяся появлением антител;
- поражение организма вирусом иммунодефицита;
- тканевая несовместимость будущей мамы и плода;
- выработка аутоиммунных антител;
- депрессивные расстройства, стрессовые ситуации;
- частые рецидивы цитомегаловируса, герпеса.
Клеточный иммунитет — устанавливается количество лейкоцитов, пропорции белых кровяных клеток в лейкограмме, оценивается индекс пролиферативной активности;
Фагоцитоз;
Определение уровня антител в крови;
Гуморальный иммунный ответ — смотрят выработку иммуноглобулинов к чужеродному антигену, обращают внимание на уровень антител, содержание в крови B-лейкоцитов, определяют циркулирующие иммунокомплексы в крови.
Некоторые родители настаивают на проведении иммунограммы перед прививкой. Тестирование необязательно, если у ребенка отсутствуют родовые осложнения. Тестирование необходимо при лейкопении — снижении уровня лейкоцитов в крови.
Результаты анализа готовы через 3-5 дней. Обычно врачи утверждают, что одного исследования недостаточно — желательно повторить иммунограмму спустя пару недель, так как исследование показывает более точные результаты в динамике.
Иммунный статус человека изучают с применением различных методик и тестов. Выделяют два основных вида исследований: иммуноферментный анализ (ИФА) и радиоиммунный анализ (РИА). Для изучения иммунного статуса применяют определенные тест-системы. При радиоиммунном анализе результаты измеряют на счетчиках радиоактивности.
- наследственные нарушения в функционировании иммунной системы;
- обильные кровопотери;
- вирусные и паразитарные инфекции различной этиологии (сифилис, лямблиоз, гепатиты герпес и другие);
- онкологические заболевания;
- патологии эндокринной системы;
- физиологические нарушения иммунной системы (при беременности, в старческом и детском возрастах);
- аутоиммунные заболевания;
- ВИЧ инфекции;
- пневмонии с частыми рецидивами;
- продолжительные грибковые инфекции;
- хронические воспалительные процессы;
- гнойные поражения кожных покровов;
- сильные эмоциональные потрясения, затяжные депрессии;
- длительное пребывание в местах с загрязненной экологией.
Исследование иммунного статуса особенно важно при обследовании пациентов с ВИЧ-инфекцией. Результаты анализов позволяют оценить степень поражения защитной системы организма
Исследование иммунограммы облегчает подбор препаратов для лечения и выбор направления терапии. Снижение защитной функции может привести к развитию тяжелых заболеваний. При длительном нарушении самочувствия рекомендуется сдать анализ крови на иммунитет и проверить состояние здоровья.
Вопрос 3. Антигены микроорганизмов.
Антигены
бактерий:
-
-
Н-
антиген (жгутиковый) входит в состав
жгутиков бактерий. Это белок флагеллин; -
О-антиген
(соматический) связан с бактериальной
клеточной стенкой. У грамотрицательных
бактерий это липополисахарид клеточной
стенки. Он термостабилен, не разрушается
после обработки формалином и этанолом; -
К-антиген
(капсульный) расположен на внешней
стороне клеточной стенки. По
чувствительности к температуре
К-антиген разделяют на А-, В- и L-антигены.
А-антигены наиболее стабильные,
выдерживают кипячение в течение 2-х
часов, В-антигены выдерживают нагревание
при температуре 60 градусов в течение
часа иL-антигены быстро
разрушаются.
-
Антигены
бактериальных токсиновявляются
полноценными, если представляют собой
белки.
Антигены
вирусов:
-
у
простых вирионов антигены связаны с
нуклеокапсидом, по химическому составу
они являются рибонуклеопротеидами или
дезоксирибонуклеопротеидами, являются
растворимыми соединениями, их обозначают
S-антигены, -
у
сложноорганизованных вирионов различают
S- иV-антигены.S- связаны с нуклеокапсидом,V-антигены – с гликопротеидами
внешней оболочки, это гемагглютинин и
нейраминидаза.
Клеточный
Осуществляется за счет захвата особыми клетками (антигенпрезентирующими) микроорганизмов либо токсинов. В этих клетках происходит их частичная нейтрализация и анализ. Затем информация о возбудителе поступает от этих клеток к фагоцитам (Т-киллерам, NK-клеткам), которые «настраиваются» на уничтожение соответствующего возбудителя, либо мутировавших клеток.
Процесс настройки заключается в изменении либо появлении новых рецепторов на мембране лейкоцитов. Это позволяет им найти и уничтожить болезнетворные микробы, зараженные вирусами клетки, либо переродившиеся в злокачественные.
Клеточны ответ может протекать не только в форме фагоцитоза. Т-киллеры при обнаружении опасной клетки могут выделить на ее мембрану особые белки – перфорины. При взаимодействии с клеткой мишенью они создают отверстия в ее оболочке, через которые Т-киллер впрыскивает токсины, уничтожающие клетку.
Еще один механизм защиты – запуск процесса апоптоза, то есть самоуничтожения клетки, переродившейся в опухолевую либо зараженную вирусом. Осуществляется также за счет выделения специфических белков. Они соединяются с мембраной клетки-мишени и запускают процесс самоуничтожения. Так уничтожается подавляющее большинство раковых клеток, которые ежедневно образуются в организме в больших количествах.
Другие факторы иммунитета
Каждый вид защиты организма от чужеродных агентов обладает своими, скажем так, исполнителями, которые стремятся уничтожить патогенное образование или хотя бы воспрепятствовать его проникновению в систему. Повторим, что иммунитет по одной из классификаций бывает:
1. Врожденный.
2. Приобретенный. Бывает активным (появляется после прививок и некоторых заболеваний) и пассивным (возникает в результате передачи антител младенцу от матери или введения сыворотки с готовыми антителами).
По другой классификации иммунитет бывает:
- Естественный (включает 1 и 2 типы защиты из предыдущей классификации).
- Искусственный (это тот же приобретенный иммунитет, появившийся после прививок или некоторых сывороток).
Врожденный тип защиты обладает следующими факторами:
- Механические (кожа, слизистые, лимфоузлы).
- Химические (пот, секреты сальных желез, молочная кислота).
- Самоочищение (слезы, шелушение, чихание и прочие).
- Антиадгезивные (муцин).
- Мобилизуемые (воспаление инфицированного участка, иммунный ответ).
Приобретенный тип защиты имеет только клеточные и гуморальные факторы иммунитета. Рассмотрим их подробнее.
Оценка иммунного статуса
Иммунный статус (расширенный) — это количественная и качественная характеристика работы разных органов иммунитета и механизмов защиты.
Иммунограмма — это способ изучения иммунного статуса, исследование крови с целью определения состояния основных показателей иммунитета.
Важнейший показатель состояния — иммуноглобулины:
- IgA — оказывают сопротивление токсинам, отвечают за сохранность состояния слизистых оболочек;
- IgM — первые оказывают сопротивление патологическим микроорганизмам, по количеству можно определить наличие острого воспалительного процесса;
- IgG — их превышение указывает на хронический воспалительный процесс, так как появляются они через некоторое время после влияния раздражителя;
- IgE — участвуют в развитии аллергической реакции.
Основные методы оценки иммунологического статуса проводятся в один или два этапа. Скрининговый тест включает определение количественных показателей сыворотки крови, иммуноглобулинов, проведение аллергологических проб.
Расширенные методы оценки иммунного статуса включают изучение фагоцитарной активности нейтрофилов, Т-клеток, В-клеток и системы комплемента. На первом этапе выполняется определение дефектов иммунной системы, на втором — подробный анализ. Сколько проводится исследование по времени, зависит от клиники и способа диагностики (скрининговый тест или расширенная иммунограмма), но в среднем длительность выполнения составляет 5-15 дней.
Первый этап — ориентировочный уровень, он включает следующие тесты:
- Фагоцитарные показатели — число нейтрофилов, моноцитов, реакция фагоцитов на микробы.
- Т-система — количество лимфоцитов, соотношение зрелых клеток и субпопуляций.
- В-система — концентрация иммуноглобулинов, соотношение процента и абсолютного числа В-лимфоцитов в периферической крови.
Второй этап — аналитический уровень, он включает такие тесты, как:
- Фагоцитарная функция — активность хемотаксиса, экспрессия молекул адгезии.
- Анализ Т-системы — продукция цитокинов, активность лимфоцитов, выявление молекул адгезии, определяется аллергическая реакция.
- Анализ В-системы — исследуются иммуноглобулины lgG, секреторный субкласс lgA.
Иммунная реакция.
Основными элементами иммунной системы организма являются белые клетки крови – лимфоциты, существующие в двух формах. Обе формы происходят из клеток-предшественников в костном мозге, т.н. стволовых клеток. Незрелые лимфоциты покидают костный мозг и попадают в кровяное русло. Некоторые из них направляются к тимусу (вилочковой железе), расположенному у основания шеи, где происходит их созревание. Прошедшие через тимус лимфоциты известны как Т-лимфоциты, или Т-клетки (Т от «тимус»). В экспериментах на цыплятах было показано, что другая часть незрелых лимфоцитов закрепляется и созревает в сумке Фабрициуса – лимфоидном органе около клоаки. Такие лимфоциты известны как В-лимфоциты, или В-клетки (B от bursa – сумка). У человека и других млекопитающих В-клетки созревают в лимфатических узлах и лимфоидной ткани всего организма, эквивалентных сумке Фабрициуса у птиц.
Оба типа зрелых лимфоцитов имеют на своей поверхности рецепторы, которые могут «узнавать» специфический антиген и связываться с ним. Контакт В-клеточных рецепторов со специфическим антигеном и связывание определенного его количества стимулируют рост этих клеток и последующее многократное деление; в результате образуются многочисленные клетки двух разновидностей: плазматические и «клетки памяти». Плазматические клетки синтезируют антитела, выделяющиеся в кровоток. Клетки памяти являются копиями исходных В-клеток; они отличаются большой продолжительностью жизни, и их накопление обеспечивает возможность быстрого иммунного ответа в случае повторного попадания в организм данного антигена.
Что касается Т-клеток, то при связывании их рецепторами значительного количества определенного антигена они начинают секретировать группу веществ, называемых лимфокинами. Некоторые лимфокины вызывают обычные признаки воспаления: покраснение участков кожи, местное повышение температуры и отек за счет увеличения кровотока и просачивания плазмы крови в ткани. Другие лимфокины привлекают фагоцитирующие макрофаги – клетки, которые могут захватывать и поглощать антиген (вместе со структурой, например бактериальной клеткой, на поверхности которой он находится). В отличие от Т- и В-клеток эти макрофаги не обладают специфичностью и атакуют широкий спектр разных антигенов. Еще одна группа лимфокинов способствует разрушению инфицированных клеток. Наконец, ряд лимфокинов стимулирует добавочное количество Т-клеток к делению, что обеспечивает быстрое возрастание числа клеток, которые отвечают на тот же антиген и выделяют еще больше лимфокинов.
Антитела, вырабатываемые В-клетками и поступающие в кровь и другие жидкости организма, относят к факторам гуморального иммунитета (от лат. humor – жидкость). Защита организма, осуществляемая с помощью Т-клеток, называется клеточным иммунитетом, так как в ее основе лежит взаимодействие отдельных клеток с антигенами. Т-клетки не только активируют другие клетки путем выделения лимфокинов, но и атакуют антигены с помощью содержащих антитела структур на поверхности клетки.
Антиген может индуцировать оба типа иммунного ответа. Более того, в организме происходит определенное взаимодействие между Т- и В-клетками, причем Т-клетки осуществляют контроль над В-клетками. Т-клетки могут подавлять B-клеточный ответ на безвредные для организма чужеродные вещества или, наоборот, побуждать В-клетки вырабатывать антитела в ответ на вредные вещества с антигенными свойствами. Повреждение или недостаточность данной контролирующей системы может проявляться в виде аллергических реакций на вещества, обычно безопасные для организма.
Хемокины. Роль в иммунитете.
Важный
класс провоспалительных цитокинов,
необходимых для активации нейтрофилов
и моноцитов и привлечения этих клеток
в очаг воспаления, составляют хемокины
(хемотаксические цитокины). Источником
этих небольших белков
служат эндотелиальные иэпителиальные
клетки , фибробласты , нейтрофилы и моноциты .
Хемокины действуют черезрецепторы,
состоящие из семи трансмембранных
доменов и
сопряженные с G-белками . Выделяют
два основных класса
хемокинов: альфа-хемокины (например, ИЛ-8 )
и бета-хемокины(например,
макрофагальный воспалительный белок
1альфа ). Альфа-хемокины опосредуют
преимущественно хемотаксис
нейтрофилов, бета-хемокины —
хемотаксис моноцитов и лимфоцитов.
Многие из сигнальных молекул
обладают хемотаксическими
свойствами, в том числе это C5a, лейкотриен
B4 и
разнообразные низкомолекулярные цитокины .
Эта группа цитокинов получила общее
название » хемокины «
Взаимодействие антиген – антитело.
Антитела реагируют только с теми антигенами, которые индуцировали их синтез. Изменения химической или физической структуры антигенов приводят к образованию иных, видоизмененных антител. Такое прямое соответствие между антигенами и антителами известно под названием специфичности.
Пауль Эрлих (1854–1915) одним из первых указал на значение специфичности. Он предположил, что боковые цепи молекулы антигена подходят к рецепторным участкам в молекуле антитела, как ключ к замку. Позже К.Ландштейнеру (1868–1943) удалось показать, что в антисыворотке иммунного животного (т.е. в сыворотке крови, содержащей антитела) обнаруживаются антитела, способные различать молекулы антигенов с одинаковой молекулярной массой и одинаковым набором атомов, но отличающиеся друг от друга пространственной структурой.
В настоящее время представление о том, что комплементарность структуры определенного участка антигена и активного центра антитела определяет специфичность их взаимодействия, является общепризнанным.
От чего зависит?
Продолжительность иммунитета зависит от иммуногенности возбудителя, то есть его способности активировать иммунный ответ. Если особь заразилась инфекцией и переболела, она получает натуральный активный иммунитет. Если была получена вакцина, иммунитет будет также активным, но искусственным. Оба класса реакции – самые продолжительные из возможных.
Относительно недолговременный иммунитет формируется при получении младенцем от материнского организма антител в период нахождения в утробе. Эти антитела – залог здоровья малыша в первые несколько месяцев после рождения. Иммунитет, полученный таким образом, пассивен, а в силу своего происхождения считается натуральным.
Пассивный искусственный можно получить, если был поставлен укол сыворотки, в которой присутствуют антитела против некоторой микроскопической формы жизни или ядовитого соединения. Эффективность инъекции сохраняется несколько недель, после чего полностью пропадает.
Стерильность: актуально ли?
Выделяют стерильный иммунитет и не являющийся таковым. Стойкость к возбудителям заболеваний формируется, если человек перенес инфицирование. В ходе ответа организма основной процент патологических форм жизни уничтожается, но не всегда микробы выводятся бесследно. В ряде случаев некоторое количество сохраняется в организме. Таким возбудителям не свойственно размножение, агрессия. Состояние называют нестерильным иммунитетом, обеспечиваемым невысокой концентрацией возбудителя в человеческом организме. Этот случай сопряжен с опасностью рецидива, если иммунитет ослабевает. Локализовать, победить болезнь обычно довольно просто, поскольку внутренние системы на клеточном уровне знают, как бороться с проблемой.
Стерильный иммунитет – такое состояние, когда возбудитель устраняется бесследно. Он формируется при получении вакцины. Такой появляется, например, если человек переболеет гепатитом А на фоне заражения вирусом.